
ページ右下のチャットよりお問い合わせください。
受付時間:9:00~17:30
(土・日・祝祭日及び当社休日を除く)
化学療法歴のあるFGFR2融合遺伝子陽性の治癒切除不能な胆管癌患者を対象としたコホートAにおいて、副作用は107例中101例(94.4%)に認められました。
ピンチで拡大できますn(%)
n(%)
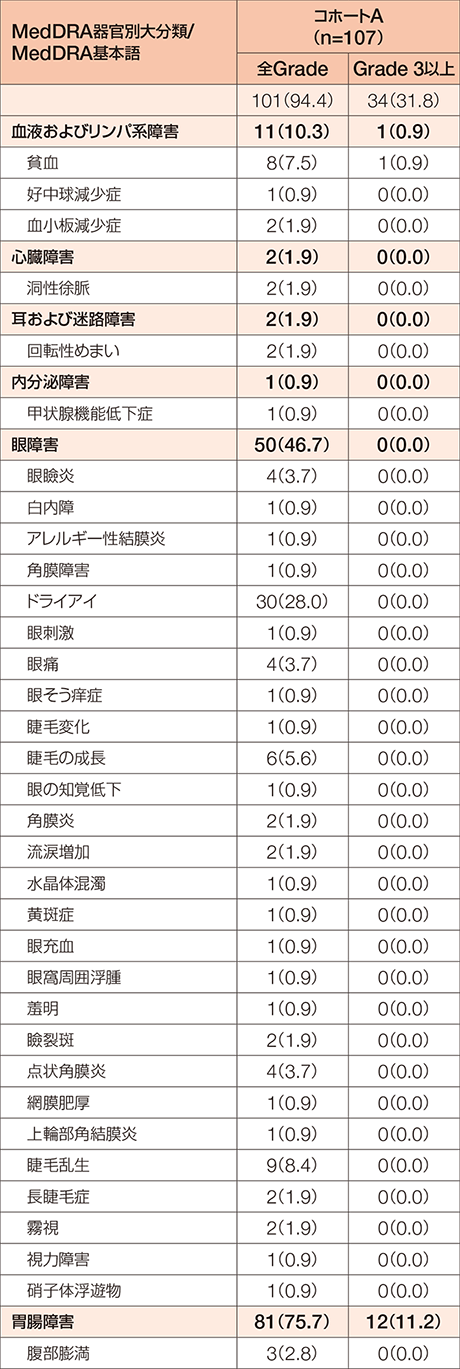
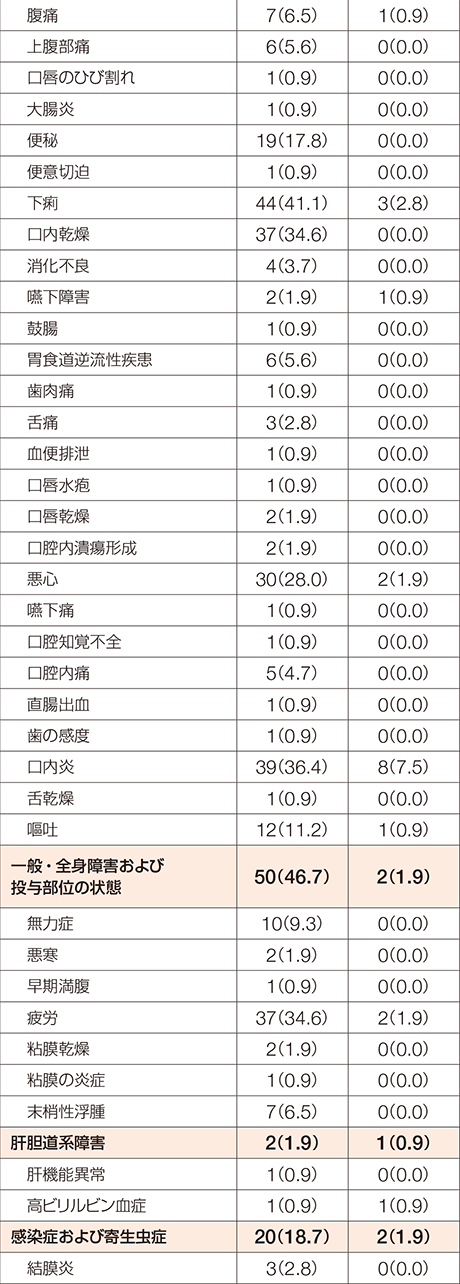
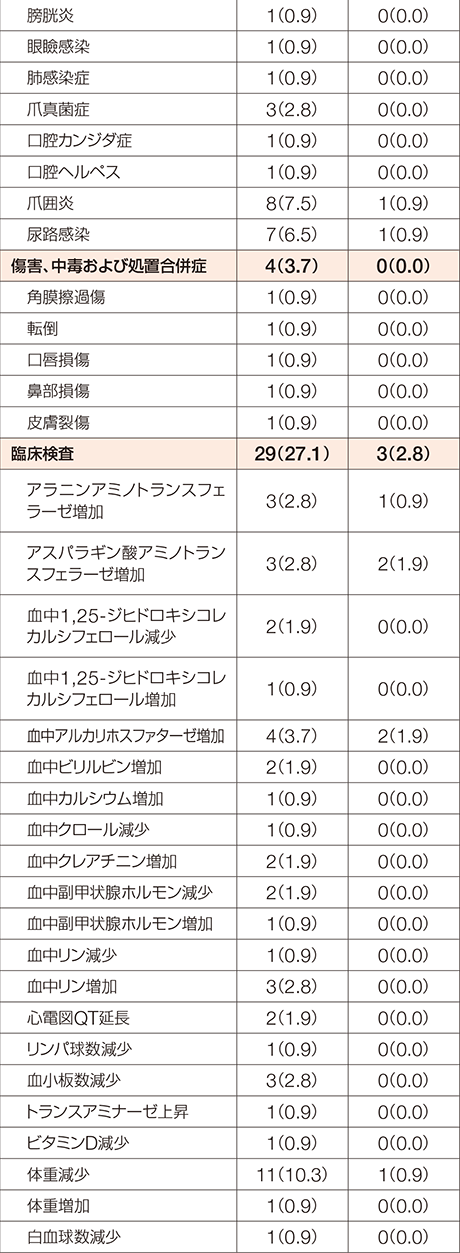
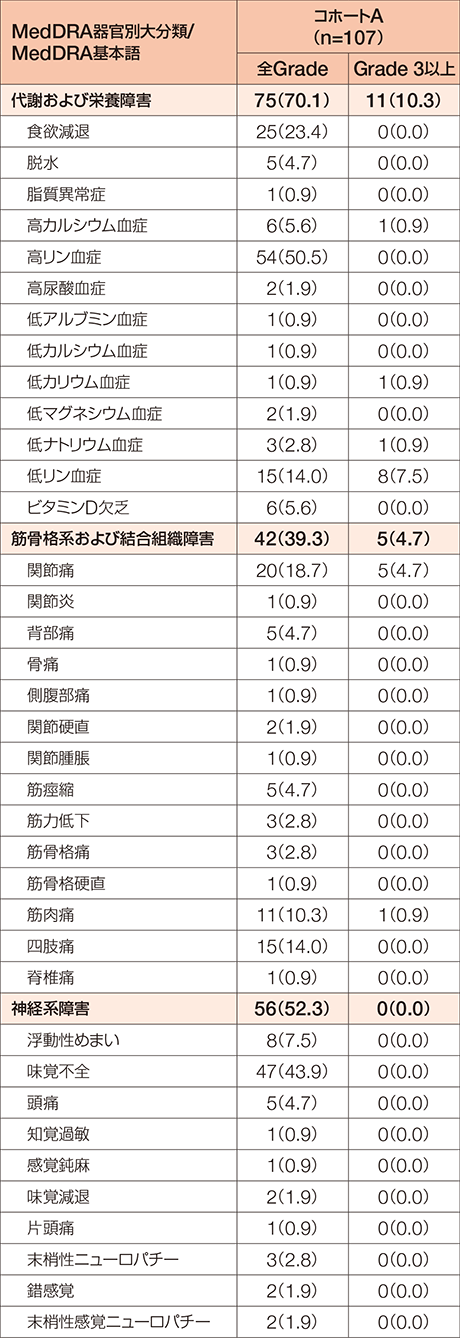
MedDRA/J version 24.0
NCI-CTCAE v4.03
NCI-CTCAEに掲載されていない高リン症については下記の定義に準じてGrade 1~4で評価した。
Grade 1:軽度;無症状又は軽度の症状;臨床的又は診断学的所見のみで処置を要さない
Grade 2:中等度;最小限の局所的又は非侵襲的な処置を要する;年齢相応の日常生活動作に支障がある
Grade 3:高度又は臨床的に重要であるが直ちに生命を脅かすことはない;入院又は入院期間の延長を要する;障害又は機能不全;日常生活動作の身辺動作に支障がある
Grade 4:生命を脅かす転帰を伴う;緊急処置を要する
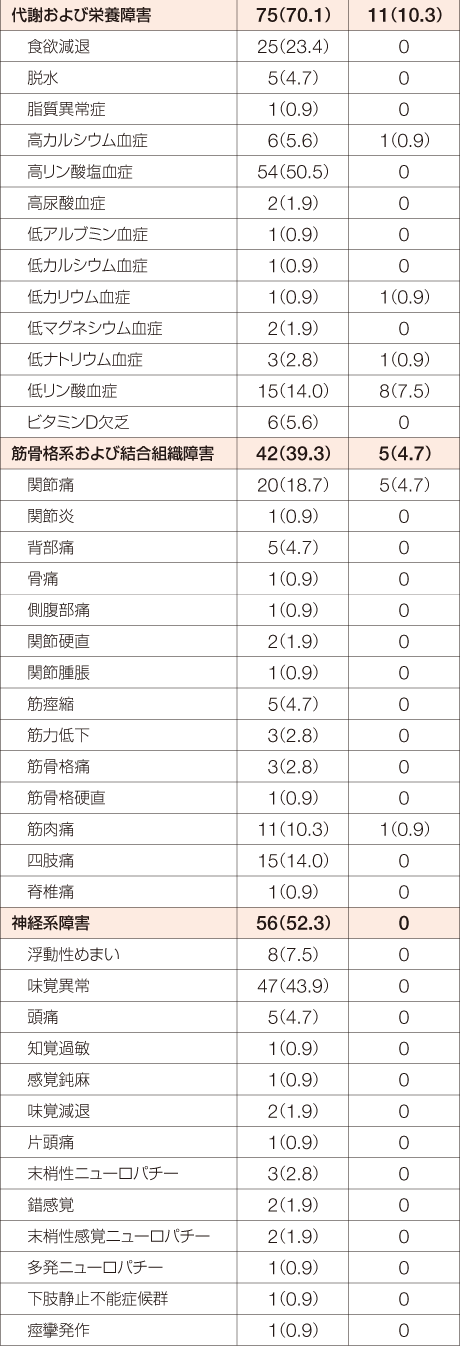
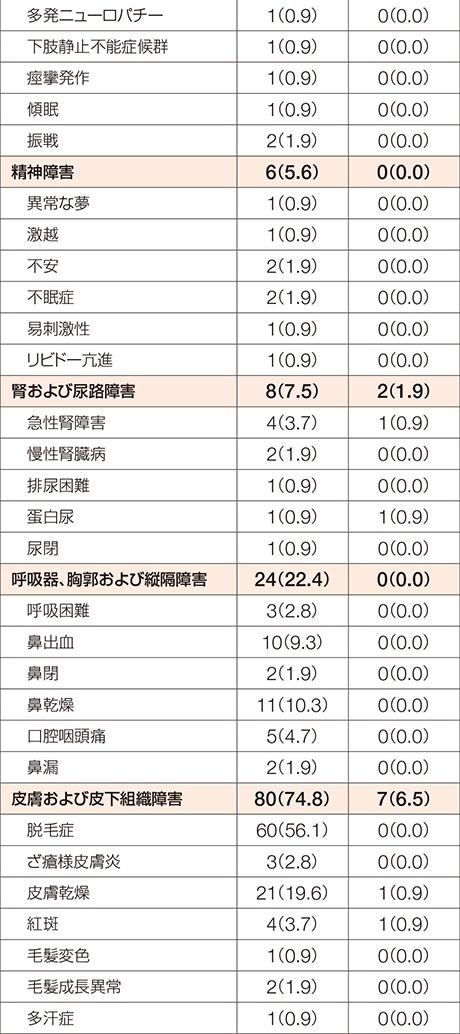
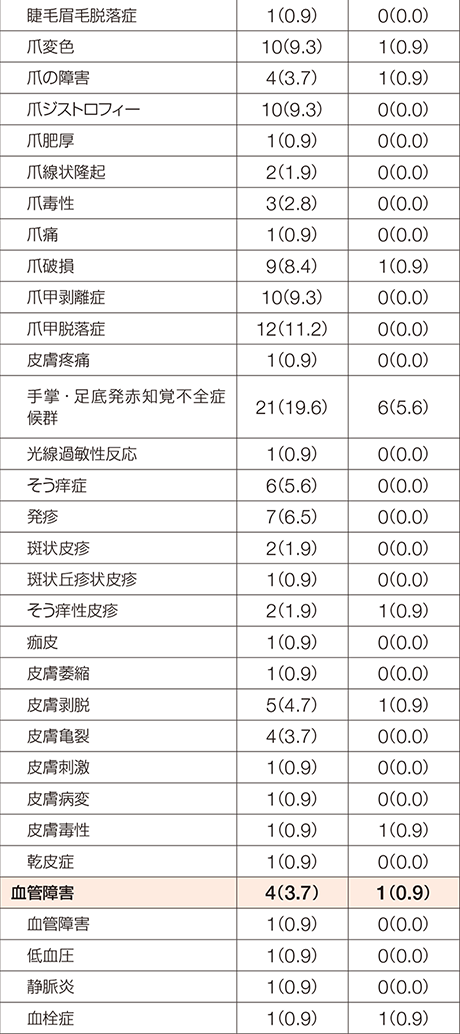
FGFR1融合遺伝子陽性の骨髄性又はリンパ性腫瘍を有する患者を対象とした本試験において、副作用は41例中40例(97.6%)に認められました。
ピンチで拡大できますn(%)
n(%)
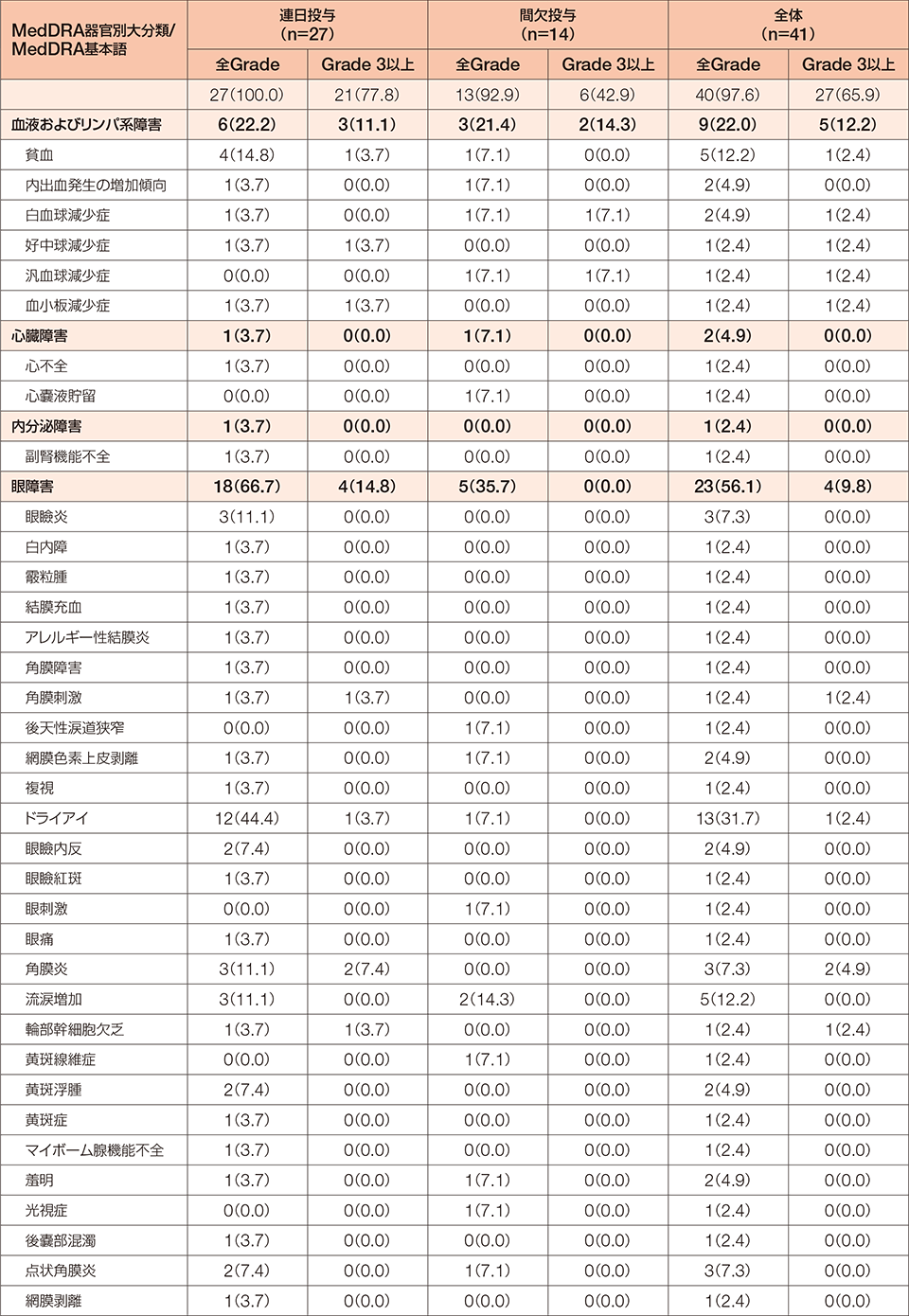
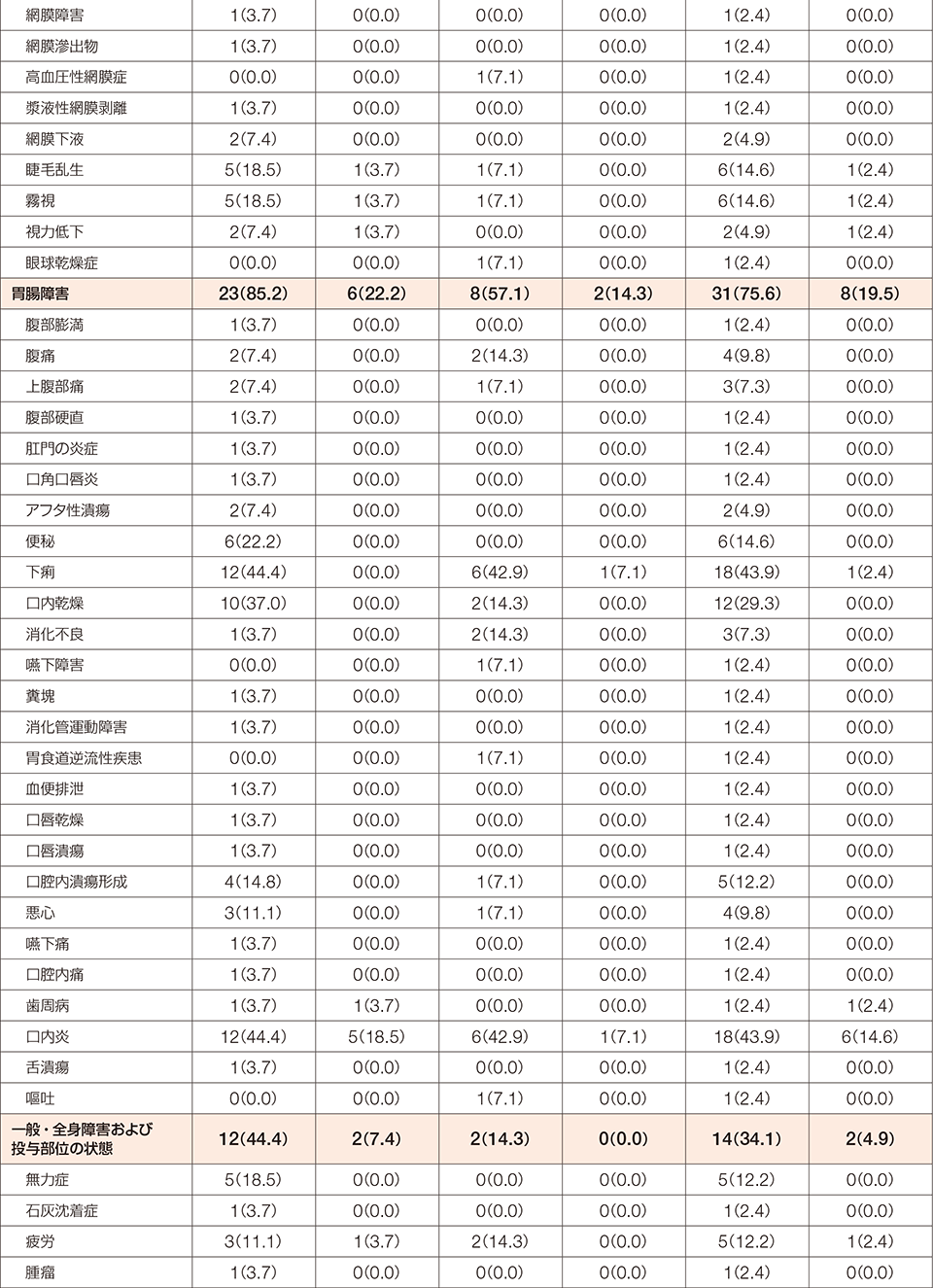
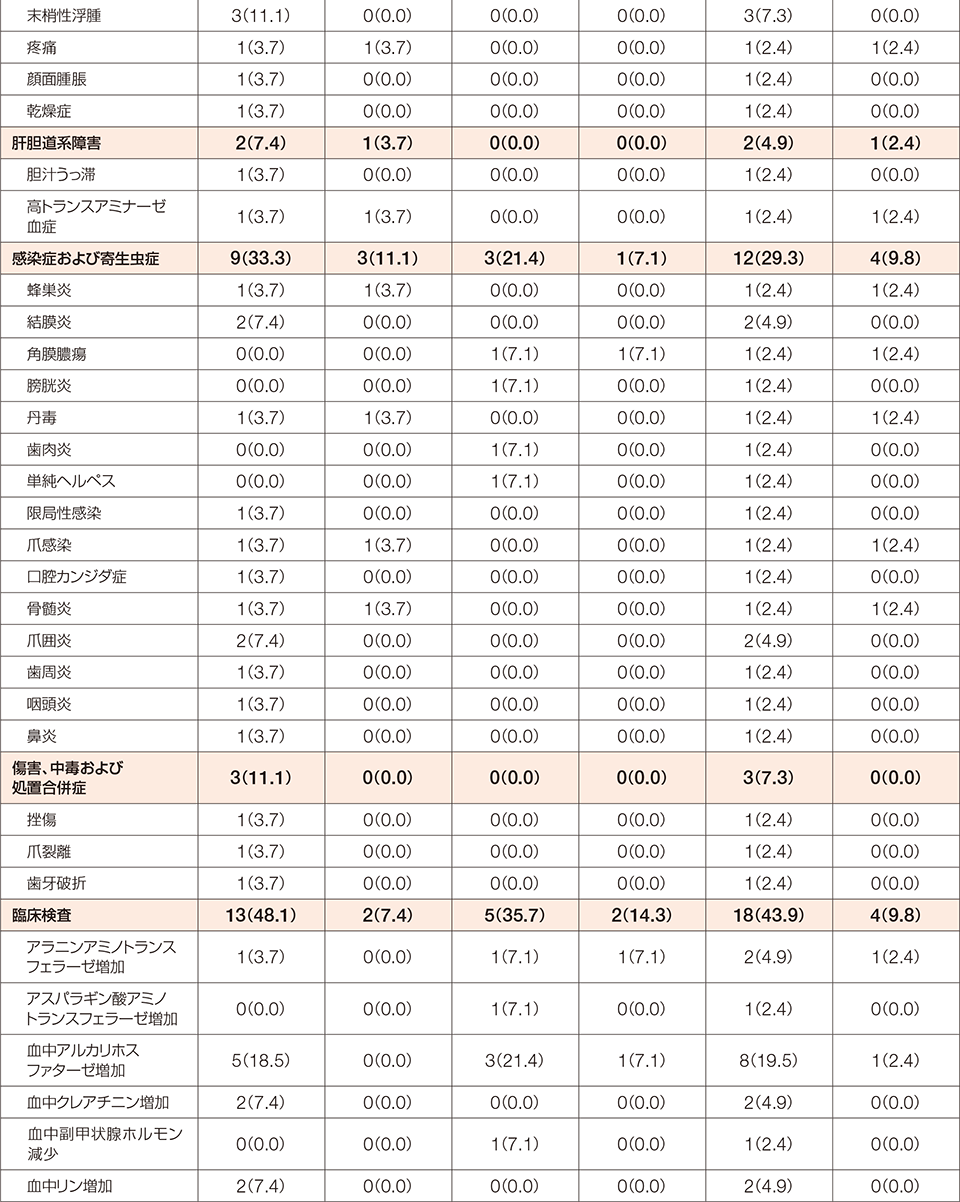
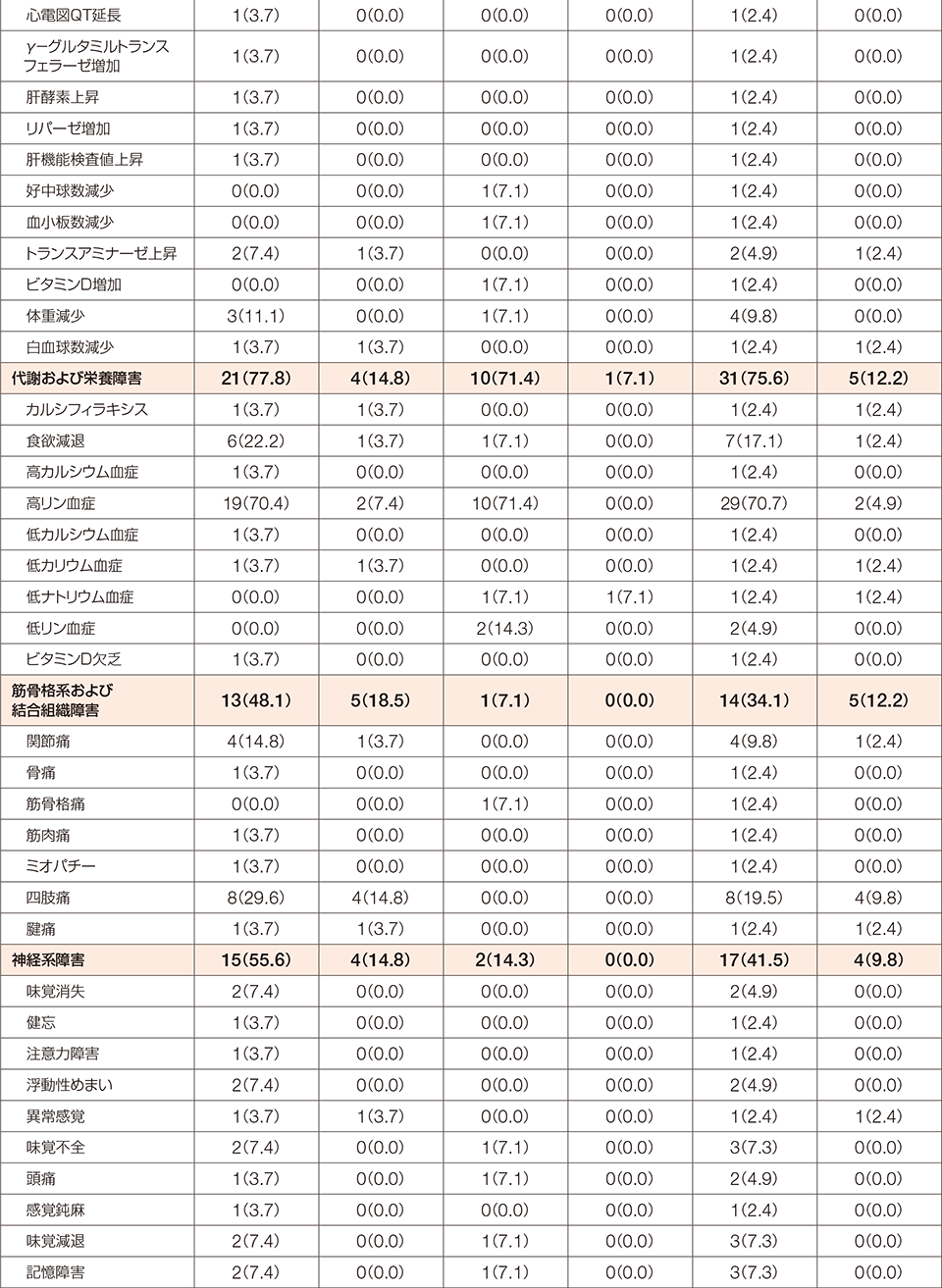
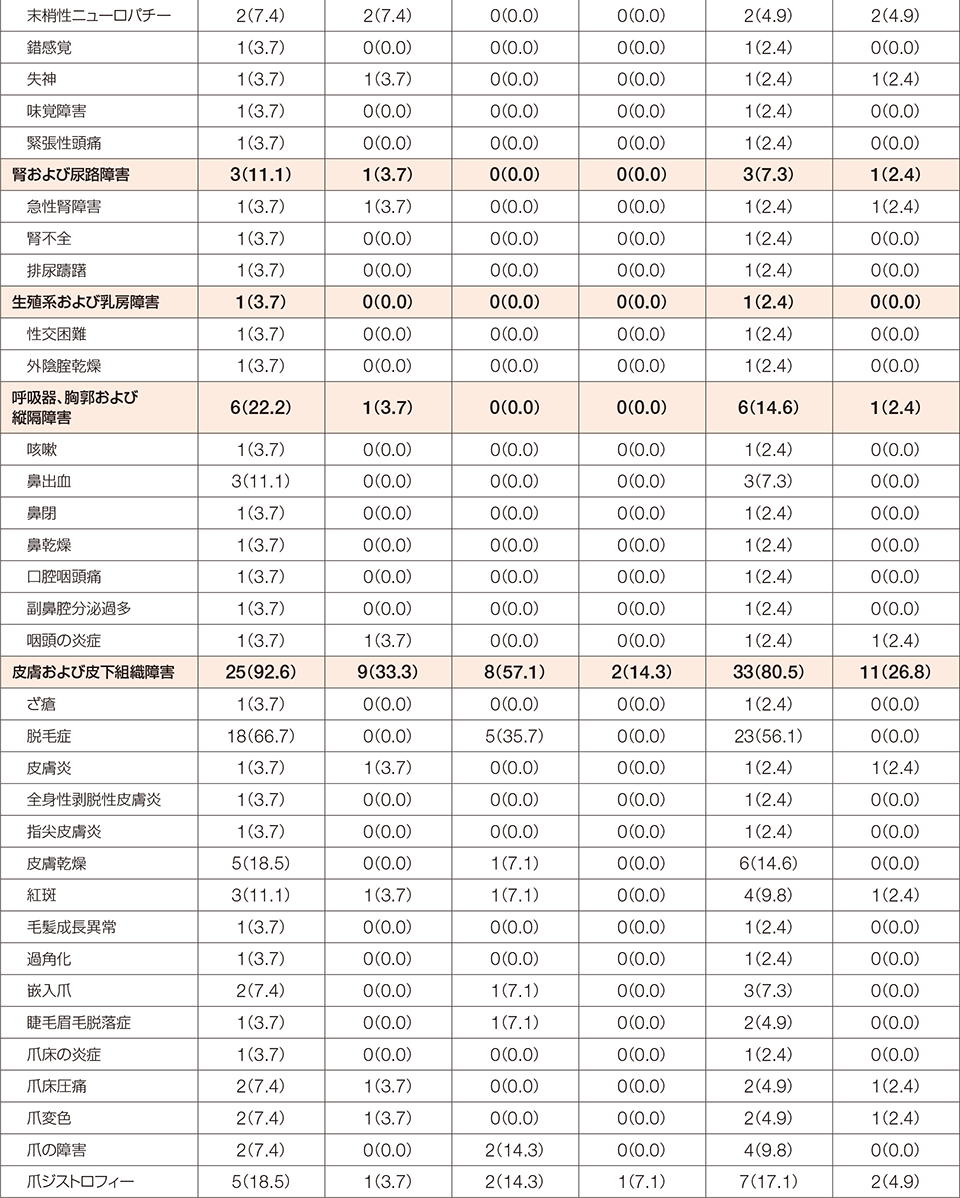
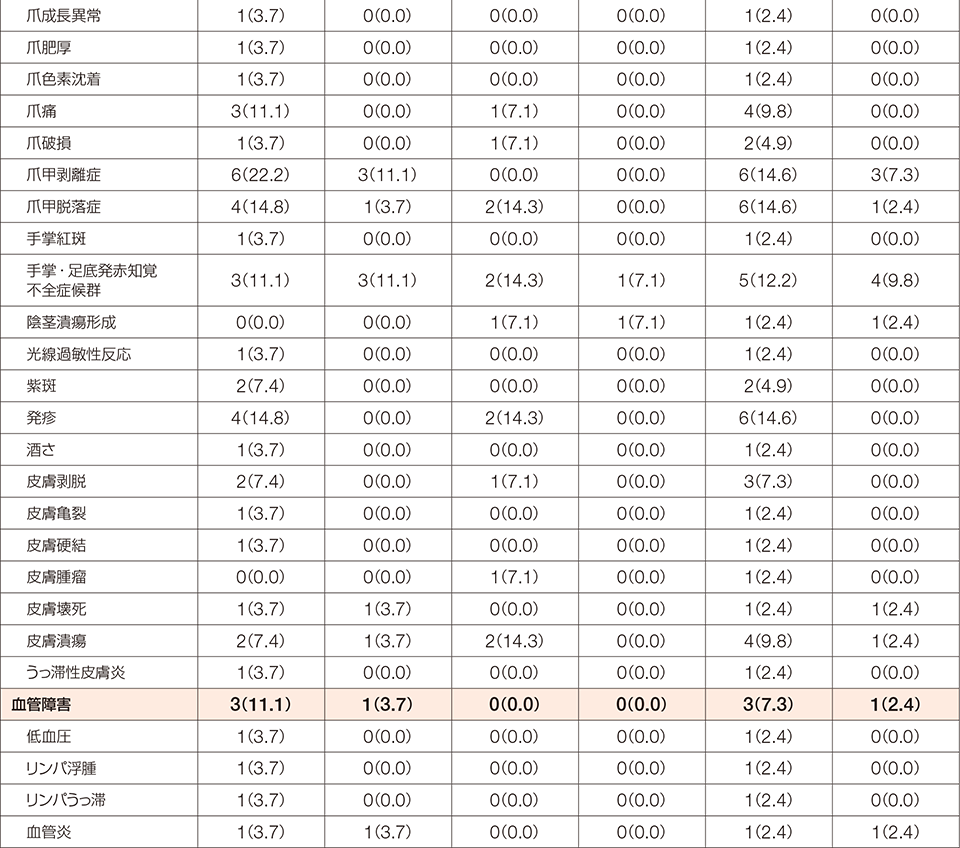
MedDRA/J version 24.0
NCI-CTCAE v4.03
注)本試験結果には一部承認外の用法及び用量による症例を含むが、承認時に評価された資料であるため掲載。本剤の承認された用法及び用量は下記電子添文の抜粋を参照。
6. 用法及び用量
<がん化学療法後に増悪したFGFR2融合遺伝子陽性の治癒切除不能な胆道癌>
通常、成人には、ペミガチニブとして1日1回13.5mgを14日間経口投与した後、7日間休薬する。これを1サイクルとして投与を繰り返す。なお、患者の状態により適宜減量する。
<FGFR1融合遺伝子陽性の骨髄性又はリンパ性腫瘍>
通常、成人には、ペミガチニブとして1日1回13.5mgを経口投与する。なお、患者の状態により適宜減量する。

ページ右下のチャットよりお問い合わせください。
受付時間:9:00~17:30
(土・日・祝祭日及び当社休日を除く)
これより外部のWebサイトに
移動します。
よろしければ下記URLを
クリックしてください。