臨床成績:骨髄性又はリンパ性腫瘍
国際共同第II相試験(FIGHT-203試験:日本人を含む海外データ)
本試験結果には一部承認外の用法及び用量によるデータを含みますが、承認時に評価された資料であるため掲載します。
承認時評価資料:国際共同第Ⅱ相試験(INCB 54828-203試験)
FGFR1融合遺伝子陽性の骨髄性又はリンパ性腫瘍におけるペマジールの有用性

再生時間08:43
ペマジールの国際共同第Ⅱ相試験FIGHT-203について、動画でご紹介しています。
試験概要

治験責任(分担)医師判定に基づく完全奏効率(CRR)、奏効率(ORR)【主要評価項目、副次評価項目】
治験責任(分担)医師判定に基づくCRは、全体40例のうち25例、連日投与集団27例のうち18例が達成し、CRRは全体では62.5%(95%CI:45.80, 77.27)、連日投与集団では66.7%(95%CI:46.04, 83.48)でした。
治験責任(分担)医師判定に基づく奏効(CR+PR)は、全体40例のうち29例、連日投与集団27例のうち21例が達成し、ORRは全体では72.5%(95%CI:56.11, 85.40)、連日投与集団では77.8%(95%CI:57.74, 91.38)でした。
治験責任(分担)医師判定に基づくCRR及びORR:全体、連日投与、有効性評価可能集団
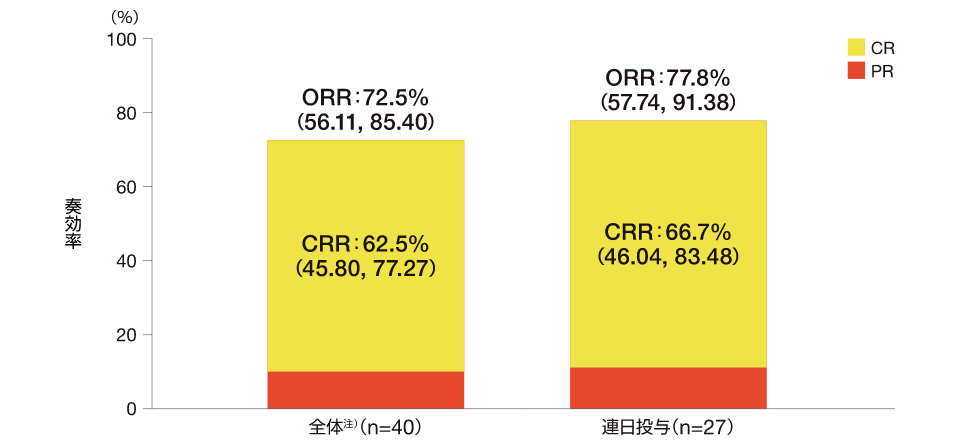
・治験責任(分担)医師判定に基づくCRは、間欠投与集団13例のうち7例が達成し、CRRは53.8%(95%CI:25.13, 80.78)でした。
・治験責任(分担)医師判定に基づくCR又はPRは、間欠投与集団13例のうち8例が達成し、ORRは61.5%(95%CI:31.58, 86.14)でした。
( )は95%CI
95%CIは、二項分布に対する直接確率検定に基づき算出した。
注)全体には一部承認外の用法及び用量による症例を含む。

・治験責任(分担)医師判定に基づく間欠投与集団のCRに至る期間中央値は3.48ヵ月(最小値, 最大値:1.4, 5.7)でした。
a CRに至る期間(ヵ月)=(最初にCRと判定された日-初回投与日+1)/30.4375
注)全体には一部承認外の用法及び用量による症例を含む。
細胞遺伝学的完全奏効率(CCyRR)及び細胞遺伝学的部分奏効率(PCyRR)【副次評価項目】
全体40例において、治験責任(分担)医師判定に基づく細胞遺伝学的完全奏効(CCyR)と判定された患者は28例(70.0%、95%CI:53.47, 83.44)、細胞遺伝学的部分奏効(PCyR)と判定された患者は6例(15.0%、95%CI:5.71, 29.84)でした。連日投与集団27例において、治験責任(分担)医師判定に基づくCCyRと判定された患者は20例(74.1%、95%CI: 53.72, 88.89)、PCyRと判定された患者は4例(14.8%、95%CI:4.19, 33.73)でした。
治験責任(分担)医師判定に基づくCCyRR及びPCyRR : 全体、連日投与、有効性評価可能集団
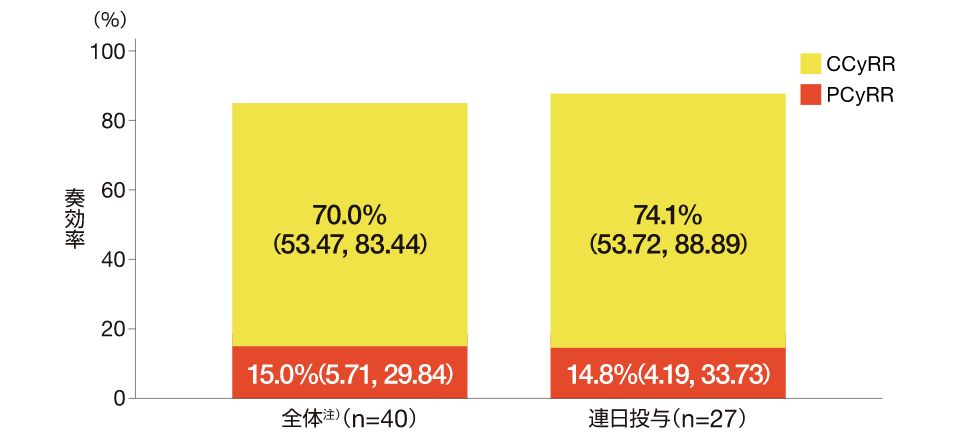
( )は95%CI
CCyRR及びPCyRRは、細胞遺伝学的最良総合効果に基づく。
95%CIは、二項分布に対する直接確率検定に基づき算出した。
注)全体には一部承認外の用法及び用量による症例を含む。
【参考】
細胞遺伝学的奏効の判定基準
・完全(CCyR):20個以上の分裂中期細胞を用いた従来の核型分析又は蛍光in situハイブリダイゼーション法(FISH)により、8p11転座を有する分裂中期細胞が0%であることが認められる。
・部分(PCyR):20個以上の分裂中期細胞を用いた従来の核型分析又はFISHにより、8p11転座を有する分裂中期細胞がベースライン値から50%以上減少していることが認められる。
無増悪生存期間(PFS)【副次評価項目】
全体40例及び連日投与集団27例において、治験責任(分担)医師判定に基づくPFSの中央値はいずれも未到達(95%CI:NE, NE)であり、PFSのKaplan-Meier推定値は、全体では3ヵ月時点で94.1%(95%CI:78.5, 98.5)、6及び9ヵ月時点でいずれも83.8%(95%CI:65.0, 93.0)、12ヵ月時点で79.1%(95%CI:58.6, 90.2)、連日投与集団では3ヵ月時点で95.7%(95%CI:72. 9, 99.4)、6、9及び12ヵ月時点でいずれも91.3%(95%CI:69.5, 97.8)でした。
治験責任(分担)医師判定に基づくPFS:全体、連日投与、有効性評価可能集団

PD:進行、NE:評価不能
a 95%CIはBrookmeyer and Crowley法を用いて算出した。
注)全体には一部承認外の用法及び用量による症例を含む。
PFSの打ち切りの定義は以下のとおりとした:
・データカットオフ時点で生存し、PDが確認されなかった患者は、データカットオフ日前の最後の腫瘍評価日にて打ち切り
・他の薬剤による治療を開始した患者又は造血幹細胞移植(SCT)を受けた患者は、他の薬剤による治療開始前又はSCT前の最後の腫瘍評価日にて打ち切り
治験責任(分担)医師判定に基づくPFSのKaplan-Meier曲線:全体、連日投与、有効性評価可能集団
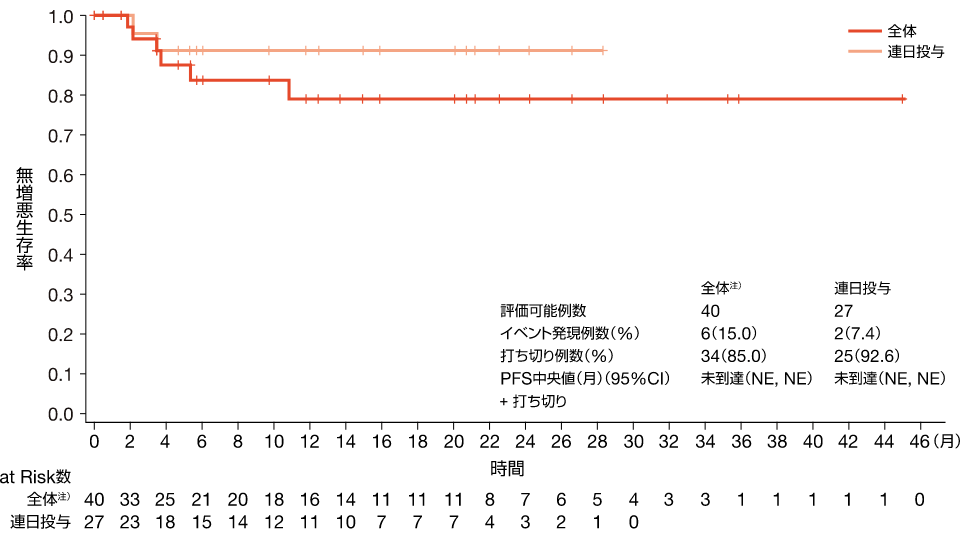
NE:評価不能
95%CIはBrookmeyer and Crowley法を用いて算出した。
注)全体には一部承認外の用法及び用量による症例を含む。
全生存期間(OS)【副次評価項目】
全体40例及び連日投与集団27例において、データカットオフ時点でそれぞれ31例(77.5%)及び24例(88.9%)が生存しており、最後に生存が確認された日をもって打ち切りとしました。OSは全体及び連日投与集団いずれも中央値未到達(95%CI:NE, NE)でした。 OSのKaplan-Meier推定値は、全体では3、6、9及び12ヵ月時点でそれぞれ94.9%(95%CI:81.0, 98.7)、86.2%(95%CI:69.8, 94.0)、82.7%(95%CI:65.3, 91.9)及び75.4%(95%CI:56.2, 87.0)、連日投与集団では3、及び6ヵ月時点でいずれも96.2%(95%CI:75.7, 99.4)、9及び12ヵ月時点でそれぞれ90.5%(95%CI:66.2, 97.6)及び84.0%(95%CI:57.2, 94.7)でした。
治験責任(分担)医師判定に基づくOS:全体、連日投与、有効性評価可能集団

NE:評価不能
a 95%CIはBrookmeyer and Crowley法を用いて算出した。
注)全体には一部承認外の用法及び用量による症例を含む。
OSの打ち切りの定義は以下のとおりとした:
・本剤の投与開始から死亡日(理由は問わない)までの期間と定義した。データカットオフ時点で生存していた患者は生存が確認された最後の日にて打ち切り
安全性
<副作用>
副作用は41例中40例(97.6%)に認められ、主な副作用は高リン血症29例(70.7%)、脱毛症23例(56.1%)、下痢及び口内炎が各18例(43.9%)等でした。連日投与集団による副作用は27/27例(100%)、間欠投与集団による副作用は13/14例(92.9%)に認められました。
<重篤な副作用>
重篤な副作用は41例中6例(14.6%)に認められ、内訳は疼痛、角膜膿瘍、丹毒、トランスアミナーゼ上昇、カルシフィラキシス、高リン血症、失神、脱毛症及び急性腎障害が各1例(2.4%)でした。
<投与中止に至った有害事象>
投与中止に至った有害事象は41例中4例(9.8%)に認められ、内訳は心不全、カルシフィラキシス、多臓器機能不全症候群及び血中アルカリホスファターゼ増加が各1例(2.4%)でした。本剤と関連ありと判断された事象は、カルシフィラキシス及び血中アルカリホスファターゼ増加が各1例(2.4%)でした。
<死亡に至った有害事象>
死亡に至った有害事象は41例中3例(7.3%)に認められ、内訳は急性腎障害、多臓器機能不全症候群及び悪性新生物進行が各1例(2.4%)でした。本剤と関連ありと判断された事象はありませんでした。
6. 用法及び用量
<がん化学療法後に増悪したFGFR2融合遺伝子陽性の治癒切除不能な胆道癌>
通常、成人には、ペミガチニブとして1日1回13.5mgを14日間経口投与した後、7日間休薬する。これを1サイクルとして投与を繰り返す。なお、患者の状態により適宜減量する。
<FGFR1融合遺伝子陽性の骨髄性又はリンパ性腫瘍>
通常、成人には、ペミガチニブとして1日1回13.5mgを経口投与する。なお、患者の状態により適宜減量する。


